تعد الروابط الكيميائية هي القوة الخفية التي تمسك بزمام هذا الكون، فهي التي تحدد كيف تتفاعل المواد وكيف تتكون المركبات التي نستخدمها في حياتنا اليومية. لكن ثمة خلط شائع يقع فيه الكثيرون عند الحديث عن طبيعة هذه الروابط، وتحديداً الرابطة الأيونية، وهو ما يحتاج إلى توضيح علمي دقيق ومبسط في آن واحد.

حقيقة الروابط الأيونية وكيفية تشكلها
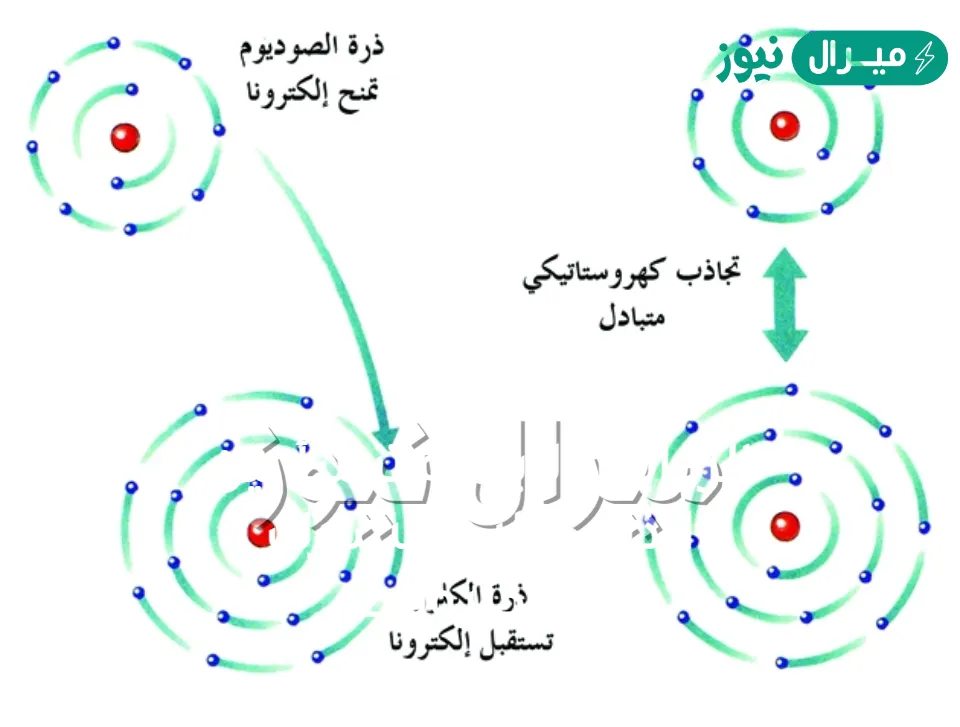
من الناحية العلمية، يسود اعتقاد خاطئ بأن الروابط الأيونية تعتمد على التشارك، بينما الحقيقة هي أن الرابطة الأيونية تقوم على مبدأ “الفقد والاكتساب” وليس “المشاركة”. تنشأ هذه الرابطة عندما يقرر أحد العناصر التخلي عن إلكتروناته لصالح عنصر آخر، مما يخلق تجاذباً كهربياً قوياً بين ذرتين مختلفتين في الشحنة.
- الاجابة : خطأ.
يُذكر أن هذا النوع من الروابط يحدث غالباً بين الفلزات واللافلزات؛ حيث تميل الفلزات إلى فقد الإلكترونات لتصبح أيونات موجبة، بينما تسعى اللافلزات لاقتناص تلك الإلكترونات لتتحول إلى أيونات سالبة.
الفرق الجوهري بين التشارك والتبادل الإلكتروني
في سياق متصل، يجب التمييز بين الرابطة الأيونية والرابطة التساهمية، فالمقولة التي تشير إلى أن الروابط الأيونية تنشأ بين الذرات التي تتشارك الإلكترونات هي مقولة غير دقيقة علمياً. إليكم النقاط الجوهرية التي توضح هذا الفرق:
الرابطة الأيونية: تعتمد على انتقال كامل للإلكترونات من ذرة إلى أخرى، مما ينتج عنه قوى جذب إلكتروستاتيكية.
الرابطة التساهمية: هي التي تقوم فعلياً على مبدأ “التشارك” حيث تساهم كل ذرة بزوج أو أكثر من الإلكترونات مع الذرة الأخرى.
طبيعة العناصر: الرابطة الأيونية تجمع عادة بين طرفين متباعدين في الخصائص (مثل الصوديوم والكلور)، بينما التساهمية تجمع غالباً بين اللافلزات المتقاربة.
لماذا يخطئ البعض في تصنيف الروابط؟
قد يعود السبب في هذا الخلط إلى تشابه الهدف النهائي لكلتا الرابطتين، وهو رغبة الذرة في الوصول إلى حالة “الاستقرار” أو ملء مدارها الخارجي. ومن المتوقع أن يساعد فهم هذا الفارق في استيعاب خصائص المواد من حولنا؛ فالمركبات الأيونية مثل ملح الطعام تمتاز بدرجات انصهار عالية وقدرة على التوصيل الكهربائي عند إذابتها، وهي خصائص تختلف تماماً عن المركبات التساهمية.
كيف تميز بين أنواع الروابط بسهولة؟
إذا كنت تدرس الكيمياء أو مهتماً بفهم طبيعة المواد، يمكنك اتباع هذه القواعد البسيطة للتفريق بينهما:
ابحث عن طرفي العلاقة: إذا كان أحدهما من يسار الجدول الدوري (فلز) والآخر من يمينه (لافلز)، فالرابطة غالباً أيونية.
راقب حركة الإلكترون: انتقال كامل يعني “أيونية”، ومساهمة متبادلة تعني “تساهمية”.
تذكر المثال الأشهر: ملح الطعام (كلوريد الصوديوم) هو النموذج المثالي للرابطة الأيونية القائمة على التجاذب لا التشارك.
خلاصة القول، إن الروابط الأيونية هي علاقة قائمة على العطاء الكامل للإلكترونات وليست مشاركة كما هو الحال في الروابط التساهمية. وفهمك لهذا الفرق هو المفتاح الأول لدراسة تفاعلات الكيمياء بشكل صحيح. ننصحك الآن بمراجعة الجدول الدوري لتحديد العناصر التي تميل لتكوين روابط أيونية بناءً على موقعها.
